Los tumores del Sistema Nervioso Central pueden ser relativamente indolentes y mantenerse silenciosos durante periodos ocasionalmente prolongados de tiempo o de crecimiento rápido y agresivo como los llamados Gliomas de “Alto grado de malignidad” que suelen ser muy destructivos en las áreas afectadas y generadores de sintomatología importante por el tipo de estructuras que suelen afectar, entre estos encontramos al llamado Glioma Anaplásico y al Glioblastoma Multiforme, a este respecto debemos recordar que cualquier tumor que se forme en las células gliales (del griego «glía», que significa pegamento), o en tejido de sostén, del cerebro se denomina “glioma”. Un tipo de glioma es el astrocitoma. Los astrocitomas toman su nombre de los astrocitos, las células en forma de estrella de las cuales crecen.
Los astrocitomas se clasifican por grado para describir su comportamiento, tratamiento y pronóstico. El sistema de gradación utiliza una escala de I a IV. Los tumores, de manera paralela, también se pueden agrupar por su ritmo de crecimiento: grado bajo (crecimiento lento), grado medio (moderado) y grado alto (rápido).
En esa escala, un glioma de grado I se considera benigno debido a su comportamiento no invasor y a su relativa localización bien delimitada, y sobre todo a su crecimiento relativamente lento, en estos casos el tratamiento quirúrgico completo puede ser curativo en el mejor de los casos. Estos tumores se diagnostican casi exclusivamente en la infancia.
Los gliomas de grado II a menudo se designan como de “bajo grado” ya que el término “benigno” no refleja al 100% su comportamiento, a diferencia de los tumores de grado I aquí hay cierta tendencia al crecimiento más rápido y los bordes de crecimiento comienzan a ser infiltrantes, aunque sea mínimamente a diferencia de los tumores de grado I que habitualmente se encuentran bien delimitados. A muchos pacientes con gliomas de grado II no se les hace ningún favor al decirles que sus tumores son benignos. Los pacientes con gliomas de grado II requieren un control consecutivo mediante resonancias magnéticas o tomografías computarizadas (MRI y CT, por sus siglas en inglés) para vigilar que el tumor no vuelva a aparecer, ya que como mencionamos anteriormente estos tumores comienzan a exhibir un crecimiento agresivo que microscópicamente se hace mínimamente invasor a diferencia de los de grado I y el control del límite quirúrgico puede ser relativamente difícil, dejando pequeños islotes de tumor que pudieran facilitar la recurrencia.
Los términos “glioma maligno” y “glioma de grado alto” comprenden tanto a los gliomas de grado III como a los de grado IV, y reflejan el hecho de que el manejo de estos tumores es bastante similar entre ellos, aunque como siempre con algunas excepciones importantes.
La palabra “Anaplásico” significa morfológicamente sin diferenciación y clínicamente altamente maligno y hace alusión a la falta de semejanza con el tejido sano. Un astrocitoma anaplásico es un tumor de grado III o grado medio que se infiltra en forma difusa en el tejido cerebral y que al microscopio confirma una anaplasia focal o dispersa y un aumento del índice de crecimiento en comparación con astrocitomas de grado I y II. El diagnóstico histológico se basa en la atipia nuclear y la actividad mitótica.
El glioblastoma o glioblastoma multiforme (“multiforme” ya no forma parte de la designación de la OMS, aunque glioblastoma aún se abrevia frecuentemente como “GBM”) es el grado más alto de tumor del tipo glioma (grado IV), es la forma más maligna de astrocitoma, y es sinónimo de glioma de grado IV. Las características histológicas que distinguen a los glioblastomas de todos los demás grados son la presencia de necrosis (células muertas) y el aumento de vasos sanguíneos alrededor del tumor. Los tumores de grado IV siempre son tumores de crecimiento rápido y con un alto nivel de malignidad.
En esta nueva era, se han explorado en forma intensiva marcadores moleculares que permitan superar la limitación en el diagnóstico histopatológico de los gliomas. El perfil de la expresión de los genes ha permitido desarrollar nuevos esquemas de clasificación molecular.
Esta clasificación según el perfil de expresión de los genes también ha revelado clases moleculares no detectadas mediante los métodos tradicionales de observación de muestras de tumor al microscopio.
Y a partir del empleo de estas técnicas de investigación se hicieron evidentes cuatro tipos moleculares definidos de glioblastomas. Estos tipos de glioblastoma específicos pueden llevar a diferentes regímenes de tratamiento. La incorporación de técnicas moleculares en los análisis de tumores de los pacientes dará la esperanza de una medicina personalizada mediante fármacos oncológicos específicos.
Aproximadamente el 50% de los gliomas son glioblastomas. Son más comunes en adultos de entre 45 y 65 años de edad, y afectan a más hombres que mujeres. Los glioblastomas se forman a partir de tejido cerebral normal. Pueden invadir y migrar fuera del tumor principal dentro del cerebro; no obstante, los glioblastomas rara vez se propagan a otras partes del cuerpo. Hay dos subtipos de glioblastomas: de novo (nuevo o primario) y secundario. Los tumores de novo se desarrollan rápidamente y tienden a mostrar su presencia en forma abrupta. Son los más comunes, y una forma de glioblastomas muy agresiva. Los tumores de novo representan la mayoría de los glioblastomas en personas de 55 años en adelante. Los glioblastomas secundarios se encuentran con más frecuencia en pacientes de 45 años y menos, generalmente comienzan como astrocitomas de grado bajo o medio que fueron programados genéticamente para transformarse finalmente en glioblastomas malignos de crecimiento rápido. Los astrocitomas anaplásicos aparecen con más frecuencia en adultos más jóvenes.
Los astrocitomas anaplásicos aparecen con más frecuencia en adultos jóvenes. Aproximadamente el 9% de los tumores cerebrales infantiles son glioblastomas. Estos tumores pueden ser multicéntricos ya que se ha observado que se ha observado que entre el 1 y el 7% de las personas con glioblastomas y aproximadamente el 4% de las personas con astrocitomas anaplásicos tienen varios tumores en el momento del diagnóstico.
Los tumores cerebrales no se pueden prevenir lamentablemente. La causa de estos tumores y otros tipos de tumores cerebrales se desconoce. Los genes son componentes básicos fundamentales que se encuentran en todas las células del cuerpo y que pueden sufrir mutaciones, como sucede en los fenómenos de carcinogénesis de otras partes del cuerpo. A la fecha se han identificado anomalías en los genes de diferentes cromosomas que podrían desempeñar un rol en el desarrollo de los tumores.
No obstante, aún no se sabe con certeza qué es lo que causa estas anomalías. A través de investigaciones ambientales, ocupacionales, familiares y genéticas se intentado identificar factores importantes en as Genesis de estas mutaciones para identificar los vínculos más comunes entre pacientes y determinadas lesiones. A pesar de la gran cantidad de investigaciones sobre los riesgos ambientales, no se ha encontrado ninguna causa directa. La mayoría de los tumores cerebrales no son hereditarios. Los tumores cerebrales pueden ser causados por un síndrome heredado genéticamente, como, por ejemplo, la neurofibromatosis, Li-Fraumeni, Von Hippel-Lindau, Turcott y esclerosis tuberosa, aunque estos mecanismos afectan solamente al 5% de los pacientes.
Los síntomas están relacionados con el efecto de masa ocupativa que genera la presencia y crecimiento del tumor. A medida que crece el tumor, puede interferir con las funciones normales del cerebro, reflejando en mayor o menor medida el efecto sobre las áreas especializadas del mismo. Los síntomas son una señal evidente de esta interferencia. Como el cráneo no se puede expandir en respuesta al crecimiento de un tumor, los primeros síntomas generalmente se deben a un aumento de la presión en el cerebro y desde luego a la selectividad de la localización del tumor. Los dolores de cabeza, las convulsiones, la pérdida de memoria y los cambios de comportamiento son los síntomas más comunes. También son comunes la pérdida de movimiento o sensibilidad en un lado del cuerpo, una disfunción en el lenguaje y trastornos del conocimiento del medio ambiente.
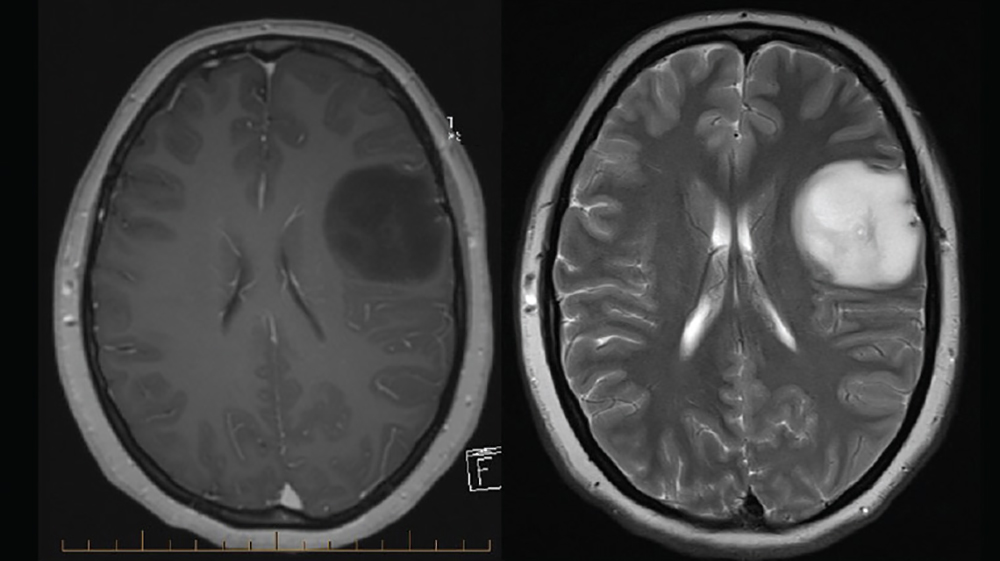
Dependiendo del tamaño y la ubicación del tumor también pueden aparecer otros síntomas. Para obtener un diagnóstico preciso, lo prudente es comenzar con un examen neurológico seguido por una RESONANCIA NUCLEAR MAGNETICA O UINA TOMOGRAFIA COMPUTARIZADA. La exploración se realizará con material de contraste que hace que el borde y los detalles del tumor sean más visibles. También es útil solicitar una espectroscopia por resonancia magnética (MRS), que mide los niveles químicos y minerales en un tumor. Esas mediciones pueden dar una sugerencia de si el tumor es maligno o benigno. También podría ayudar a distinguir entre un tumor cerebral y otros problemas médicos, como una infección (tuberculosis, parásitos, bacterias y hongos), desmielinización (una enfermedad que daña la mielina, o la vaina protectora, de las neuronas del cerebro). En la Resonancia Nuclear Magnética con contraste, los gliomas de grado alto se ven brillantes (esto se denomina realce); los gliomas de grado bajo frecuentemente no se destacan con el contraste o solo lo hacen levemente. No obstante, únicamente el examen del tejido del tumor de un paciente al microscopio puede confirmar un diagnóstico exacto.
Generalmente, el primer paso en el tratamiento de los glioblastomas es la cirugía. Con las técnicas modernas actuales, la cirugía como procedimiento generalmente es segura para la mayoría de los pacientes. Los objetivos de la cirugía son obtener tejido tumoral para el diagnóstico y la planificación del tratamiento, extirpar la mayor cantidad posible de tumor y reducir los síntomas provocados por la presencia del tumor. En algunas circunstancias, se puede realizar una biopsia en lugar de una cirugía. El tejido obtenido durante la biopsia se usa luego para confirmar el diagnóstico. El diagnóstico se basa en el cambio de estructura celular más visible y la actividad de crecimiento observada en el tejido, incluso si las características se encuentran únicamente en unas pocas células.
Los aspiradores ultrasónicos son instrumentos que pueden dividir y succionar el tumor. Actualmente los microscopios de alta potencia ayudan al neurocirujano a ver mejor el tumor.
Debido a que las células de un astrocitoma, son similares a tentáculos, crecen dentro del tejido circundante, y esto aumenta la dificultad para controlar la resección del tumor haciendo que en ocasiones no se pueden extirpar en su totalidad. No obstante, la cirugía es útil ya que la extirpación parcial puede ayudar a disminuir los síntomas y el tejido obtenido durante la cirugía confirma el tipo de tumor. Luego se usa radiación, quimioterapia o bioterapia para tratar el tumor remanente.
RADIACIÓN
En los adultos, generalmente se administra radioterapia luego de una biopsia o cirugía. Hay diferentes tipos de radiación que se pueden administrar usando diversas dosis y programas. La radiación de haz externo fraccionado convencional es la radiación “estándar” que se administra cinco días a la semana durante cinco o seis semanas.